les APPLICATIONS EN DENTISTERIE RÉGÉNÉRATIVE
DU PLatelet-RICH FIBRIN (PRF)
Toutes les techniques de chirurgies orales peuvent être conjuguées avec le PRF: les greffes osseuses
les GREFFES GINGIVALES et la pose d'implants dentaires
les APPLICATIONS EN DENTISTERIE RÉGÉNÉRATIVE
DU PLatelet-RICH FIBRIN - PRF
La plupart des thérapeutiques chirurgicales déjà existante en chirurgie orale ont été modifiées à l’aune de la technique du PRF. Mais pas seulement, des nouveaux protocoles thérapeutiques en dentisterie et en médecine ont été inventés grâce à la formidable capacité régénératrice des PRF.
Chaque scientifique ou clinicien s’efforce d’explorer les immenses potentiels de cette nouvelle thérapie et de faire évoluer les mentalités aussi vite que les protocoles.
Par exemple, les techniques chirurgicales de greffes de gencives et de greffes osseuses ont été reformatés et réinventés à l’aune des principes de la dentisterie régénérative, grâce au docteur Joseph Choukroun, son concepteur. Comme ses prédécesseurs, il a su créer tout un univers et une communauté médical qui gravite autour de ses principes qu’il a et qu’il continu d’édicter.
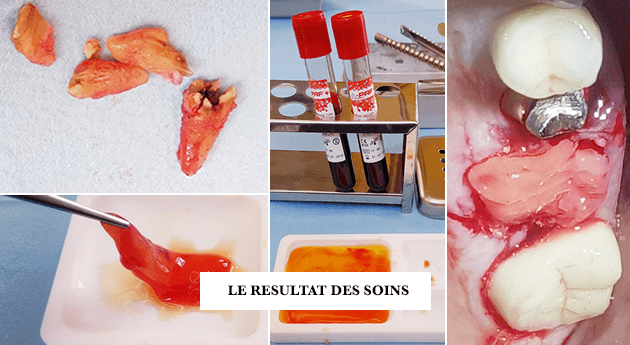
1. LE PRF POUR LA GESTION DES ALVÉOLES SUITE AUX EXTRACTIONS DENTAIRES
Note : Les protocoles de comblements alvéoles dentaires sont décrits plus spécifiquement dans le chapitre: “greffes osseuses pré implantaires“.
Les propriétés de cicatrisation et les avantages de l’utilisation de la fibrine riche en plaquettes (PRF) sont utilisés pour optimiser la cicatrisation osseuse des alvéoles vides après une extraction dentaires et réduire la perte osseuse.
Les recherches récentes ont montré que la principale cause de l’accélération de la résorption tridimensionnels de l’os alvéolaire après l’extraction d’une dent est principalement due à la réduction du flux sanguin résultant de cette perte de cette dent.
Dans l’os alvéolaire, le ligament parodontal, appelé desmodonte, contient la majeure partie de l’apport sanguin. Une fois la dent extraite et donc le ligament dentaire autour retiré, une perte osseuse rapide et radicale se produit au niveau des dents manquantes, notamment sur les minces parois osseuses buccales.
Le PRF peut être utilisé comme biomatériau de greffe unique par un comblement de l’alvéoles dentaires par des membranes a-PRF.
Le PRF peut être utilisé en combinaison avec tous les types de greffons osseux de comblement pour limiter les modifications tridimensionnelles post-extractionelles.
Le protocole qui devient le standard est décrit par le docteur Joseph Choukroun comme un mélange d’os de banque et de i-PRF. Une couverture de membranes de a-PRF vient parfaire l’ensemble.
Mais toutes les reconstructions peuvent être faites par tout types de greffe de comblement osseux et avec la plupart des biomatériaux : depuis les substituts osseux synthétique jusqu’aux autogreffes.
Pour autant les prélèvements au menton, au crâne dans sa partie pariétale ou au niveau de l’iliaque sont trop complexes. Les matériaux de comblement d’origine synthétique ou animal ou de banque osseuse sont préférables.

2. L’UTILISATION DE PRF DANS L’ÉLÉVATION DU PLANCHER DU SINUS (SINUS LIFT)
DANS LE CAS D’ATROPHIE POSTÉRIEURE DU MAXILLAIRE
Nous avons un recul de plus de trente ans depuis la première intervention d’élévation du plancher du sinus maxillaire, appelés également sinus lift ou comblement de sinus.
Les risques d’aléa restent toutefois nombreux. Mais les protocoles novateurs associant le PRF, sont des garantis d’optimisation et d’accélération de la cicatrisation. En particulier, pour des patients âgées ou affaiblies par des pathologies qui réduisent leur vascularisation et donc leur capacité à cicatriser. Le diabète même équilibré diminue la concentration vasculaire et réduit le flux sanguin en épaississant le sang. Un taux de cholestérol élevé va diminuer la capacité des cellules ostéoblastes à fabriquer de l’os. Les personnes âgées sont naturellement notre coeur de patientèle, puisque l’édentement et la résorption osseuse augmente avec l’âge. Or ces patients ont un pouvoir de régénération tissulaire qui diminue. L’apport du PRF dans ces situations est un gage d’amélioration de la cicatrisation même si l’idéal n’existe pas.
Bien que de nombreuses améliorations aient été apportées en ce qui concerne les techniques chirurgicales et le choix du biomatériau, cette procédure reste associée à de nombreux risques potentiels de complications. La plus fréquente étant la déchirure de la membrane dite de Schneider qui tapisse les parois sinusiennes. C’est cette fine membrane qui a la consistance d’une “feuille de papier toilette mouillée”, qui doit être délicatement relevée afin d’insérer, entre elle et le plancher osseux du sinus, un greffon osseux et réaliser ainsi le sinus lift ou remonté du plancher du sinus.
Le chirurgien-dentiste bien que familiarisé avec les caractéristiques anatomiques et les anomalies de la cavité du sinus maxillaire peut perforer cette membrane si fragile. Le taux de perforation important de la membrane de Schneider au cours d’un sinus lift a comme conséquence possible un risque d’infection aiguë ou chronique, comme une sinusite chronique ou une surinfection infectieuse ou inflammatoire type rhinite. La pose de membranes a-PRF pour réparer les petites effractions de cette membrane de Schneider est démontrée comme particulièrement efficace.
La loge intra sinusienne délimitée par le plancher du sinus maxillaire et la membrane de Schneider est remplie par le greffon osseux saturé de PRF sous toutes ses formes. L’apport en plaquettes sanguines et en cellules cicatricielles est considérable.
Dans les techniques chirurgicales de greffes osseuses, type sinus lift, associant le PRF, le docteur Joseph Choukroun suggère l’utilisation de S-PRF comme agent de liaison des granules d’os de banque, type allogreffes, utilisés comme greffons osseux intra sinusiens. Le S-PRF (PRF liquide dont l’agrégation a été ralenti sans anticoagulant), éventuellement associé à du A-PRF (PRF sous forme de membrane de fibrine) va finalement architecturer un treillis matriciel de fibrine autour des granules de biomatériaux. Un ajout de I-PRF pour apporter plus de macrophages, leucocytes et cellules souches peut être fait.
Tout une gamme de biomatériaux osseux est utilisée pour faire une élévation des sinus maxillaires, unilatérale ou bilatérale, appelée aussi dans sa terminologie anglo-saxonne “sinus lift”. Ce type de greffe osseuse permet de gérer l’atrophie des crêtes alvéolaires maxillaires postérieures. Les greffons osseux sont les mêmes que pour faire une reconstruction osseuse ou une greffe osseuse d’apposition suite à des extractions dentaires. Citons pour exemple: les biomatériaux de comblement de la famille des substituts osseux synthétique, les biomatériaux d’origine animale comme les xénogreffes, les biomatériaux d’origine humaine issus de donneurs vivants comme les allogreffes, les biomatériaux issues du patient-donneur comme les autogreffes, avec un prélèvement au menton ou l’angle goniaque ou crânien pariétal ou à la hanche au niveau de l’os iliaque.
Il est remarquable que des membranes de collagène sont le plus souvent utilisés comme barrière des cellules gingivales et emballage du greffon osseux.
Le développement de concentrés de plaquettes de seconde génération PRF génère de nouveaux protocoles. Des premières études ont été faites pour déterminer si le PRF pouvait être utilisée seule ?
Après dix ans d’essais cliniques, les études montrent que le PRF peut être utilisé seul comme un matériau de greffe mais qu’il doit être le plus souvent associé à des particules de greffon osseux pour améliorer le maintien de l’espace ainsi que le potentiel angiogénique dans la loge chirurgicale formé dans le sinus entre la membrane de Schneider et le plancher du sinus.
Deux niveaux d’examen peuvent être pratiqués :
- Soit un examen radiologique classique en 2D chez le dentiste au cabinet dentaire comme un panoramique dentaire.
- Soit des examens radiologiques réalisés par un praticien spécialisé en tomodensitométrie et scanner dentaire. Comme le Cone Beam qui est le meilleur examens 3D avec une irradiation plus faible que le scanner CT.
Cette exploration de la masse osseuse faciale et maxillaire par scanner en trois dimensions permet d’étudier très finement la mâchoire supérieure et la mâchoire inférieure ainsi que toute la cavité buccale afin d’identifier toutes formes d’anomalies ou une particularité anatomique.
Dans le cas des sinus lift, seuls certaines structures anatomiques nous intéressent : le maxillaire supérieur dans sa partie postérieure, les fosses nasales qui contiennent les cornets moyens et les sinus de la face. Les cavités des sinus sont toutes reliées entre elles et se composent des sinus maxillaires, du sinus de l’ethmoïde, du sinus du sphénoïde et du sinus de l’os frontal.
Un très gros cornet moyen peut obstruer la narine. Mais même si cela peut gêner la respiration tant qu’il n’y a pas d’obstruction au passage aérien sinusal cela n’a pas d’importance pour faire un sinus lift, de même que des polypes banaux.
Par contre, une image pathologique comme une opacité radiologique, signe d’une lésion infectieuse comme une sinusite maxillaire qui peut être unilatérale ou bilatérale est un frein à l’élévation de sinus. Des sinusites infectieuses aigües sont une contre-indication au sinus lift,sauf si l’intervention règle à la fois l’étiologie de la sinusite aigüe et l’élévation de sinus. Une sinusite chronique inflammatoire n’est pas forcément une contre-indication au sinus lift mais devra faire l’objet d’une réflexion conjointe entre l’ORL et le chirurgien-dentiste.
Le rôle du radiologue et prépondérant puisqu’il va diagnostiquer une éventuelle lésion tumorale, obstruction ostiale, sinusite ou polypose.
La maladie parodontale atteint les gencives et l’os alvéolaire. Au stade ultime de la parodontite, la résorption osseuse est telle que les molaires ainsi que les dents adjacentes sont entièrement déchaussées et les extractions dentaires sont inévitables. Ce thème est abordé dans le chapitre traitant de la parodontologie.
Une fois l’os alvéolaire privé des dents qu’il doit retenir, l’os maxillaire continu de se résorber jusqu’au stade d’une fine lamelle osseuse d’un ou deux millimètres. Dans ce cas, la perte osseuse est telle que le volume osseux est insuffisant pour la pose d’implants dentaires.
La solution est une augmentation du volume osseux grâce à une greffe osseuse particulière appelée élévation du plancher du maxillaire. Elle doit être réalisée à l’intérieur du sinus maxillaire avec un biomatériau vivant et vascularisé, susceptible de recevoir et d’ostéointégrer un implant dentaire.
Sinon, il reste l’alternative des implants zygomatiques.
Il y a différentes techniques chirurgicales :
- Technique de Summers ou la voie d’abord crestale : Elle est la moins invasive mais réalisée en aveugle et la moins performante.
- La technique de Caldwell-Luc ou la voie d’abord latérale : Elle est la plus invasives mais la plus commode qui consiste à traverser la paroi latérale du maxillaire pour arriver dans le sinus.
L’intervention chirurgicale a différents temps opératoires : Sous anesthésie générale ou sous anesthésie locale une incision, le décollement d’un lambeau, la pose d’un greffon nécessaire à la reconstruction osseuse et à l’augmentation du volume des parois du sinus, et pour finir des points de sutures.
Un mélange d’os de banque, de I-PRF et quelques membranes de S-PRF et de A_PRF donne un biomatériau bioactif chargé de facteurs de croissance, appelé “sticky bone” du fait de sa plasticité.
Les membranes de fibrine de A-PRF est également évoqué pour la fermeture de la fenêtre de voie d’abord latérale dite de calwell-Luc, après une élévation du plancher du sinus maxillaire.
Les membranes de fibrine de A-PRF sont fréquemment utilisé pour la réparation des perforations de la membrane de Schneider qui tapis les parois du sinus.
Le forage pour la pose d’un implant dentaire ou de plusieurs implants en titane peut être fait en simultanée avec l’élévation du plancher du sinus.
Une prothèse dentaire comme un bridge implanto-porté sera ensuite placé immédiatement après la pose.
En post opératoire, il sera prescrit un antalgique, une antibiothérapie prophylactique, des anti inflammatoires, des bains de bouche et un brossage qui évite la zone opérée.
Les suites post opératoires peuvent être un hématome ou/et un saignement.
Le risque le plus important dans l’élévation de sinus est la perforation accidentelle de la membrane de Schneider. Dans ce cas une simple inflammation de la zone peut être observée, éventuellement accompagné d’une rhinite.
Ou bien, une surinfection peut s’installer qui va nuire à la cicatrisation osseuse. Dans certaines aigus, le greffons doit être déposé et le sinus nettoyé.
Quelque fois un morceau du greffon peut se détacher du corps de la greffe et rester libre dans le sinus. Dans ce cas, plusieurs cas de figures dont a considérer :
- Soit il est totalement neutre et reste dans le sinus ;
- Soit il s’évacue de lui-même par les voies aériennes ;
- Soit il reste coincé dans l’ostium unfudibulaire et doit être retirer par endoscopie ;
- Si le morceau est trop gros pour sortir et provoque une sinusite chronique, il sera retiré par voie endoscopique grâce à une méatotomie moyenne.
L’utilisation de PRF mélangé au greffon de biomatériau réduit les suites opératoires et prévient, dans une certaine mesure, les complications :
- Le PRF donne au greffon une capacité cicatricielle plus importante qu’un simple biomatériau neutre. Les suites opératoires en sont simplifiées et raccourcis.
- Le PRF donne au greffon osseux intra sinusien cette consistance gélatineuse qui évite le phénomène de “sac de billes” avec les granules de biomatériaux qui se déversent dans le sinus. Le risque qu’un morceau se détache est amoindri.
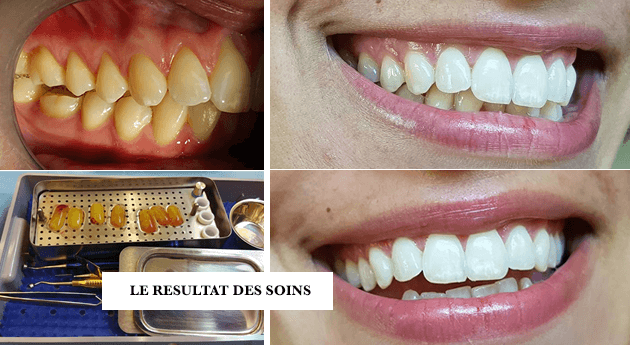
3. L’UTILISATION DU PRF POUR LE TRAITEMENT DES RÉCESSIONS MUCO-GINGIVALES
La nouvelle technique chirurgicale de régénération des tissus mous (gencive attachée et muqueuse) baptisée FASTP (Fibrin Assisted Soft Tissue Promotion) apporte des améliorations notables en chirurgie esthétique et plastique du contour gingival (chirurgie muco-gingivale)
Les résultats des nombreux essais cliniques randomisés ont mis en évidence son aptitude marquée à favoriser la cicatrisation des plaies des tissus mous. Cette propriété est utilisée pour accélérer la régénération des récessions muco-gingivales.
Un nouveau concept chirurgical est introduit après des années d’expérience clinique avec le PRF, appelée technique FASTP ou “Fibrin Assisted Soft Tissue Promotion” pouvant se traduire par «Optimisation de régénération des tissus mous induit par la fibrine».
Le principe chirurgicale est une introduction de membranes de fibrine de A-PRF grâce à une tunnélisation dans la muqueuse (avec ou sans apport de gencive attachée prélevée au palais) associée à une traction des tissus mous.
Cette traction réalisée, grâce à des points de sutures complexes (Apical Mattress), conjuguée à l’induction de la régénération tissulaire, grâce au PRF, conduit a un recouvrement des récessions muco-gingivales optimales.


4. L’UTILISATION DU PRF POUR LA RÉGÉNÉRATION PARODONTALE
Au cours des 20 dernières années, on a observé une augmentation de la prévalence des parodontopathies dus en particulier à l’accroissement de la longévité de la vie.
La régénération des défauts infra-osseux et des furcations des racines dentaires a été réalisée au moyen d’agents biologiques et des facteurs de croissance contenus dans les PRF.
Celles-ci font suite à une série d’études pionnières utilisant des membranes de collagène barrières, qui ont d’abord établi le concept de régénération tissulaire guidée (GTR) avec ou sans divers biomatériaux de greffe osseuse.
Les facteurs de croissance et les agents biologiques ont ensuite été introduits en tant qu’agents de régénération potentiels pour les défauts infra osseux péri radiculaires et des furcations.
Environ 20 ans après l’introduction dans l’arsenal thérapeutique des facteurs de croissance dérivé des concentrés plaquettaires de première génération comme le PRP, le PDGF ou les dérivés de matrice d’émail (EMD), c’est aujourd’hui les concentrés plaquettaires de deuxième génération comme le Plasma Riche en Fibrine (PRF) qui sont étudiés pour la régénération tissulaire des résorptions du parodonte.
Le PRF a récemment été utilisé dans le traitement des parodontites. Les membranes de fibrine de A-PRF contiennent des facteurs de croissance autologues en concentration supra-physiologique. La forme de membraneuse est commode à insérer dans les lésions angulaires osseuses.
Il a également été démontré que le réseau de fibrine servait de matrice provisoire permettant la création d’espace, soutenant l’angiogenèse et la formation de caillots sanguins dans les poches parodontales.
Les essais cliniques randomisés portant sur l’utilisation de PRF pour la régénération et la réparation des défauts infra-osseux et des furcations sont probants.
Les études comparatives démontrent que cette modalité de régénération réduit les profondeurs des poches parodontales et augmente le niveau d’attachement gingival clinique lorsqu’elle est utilisée seule ou en combinaison avec d’autres biomatériaux parodontaux.
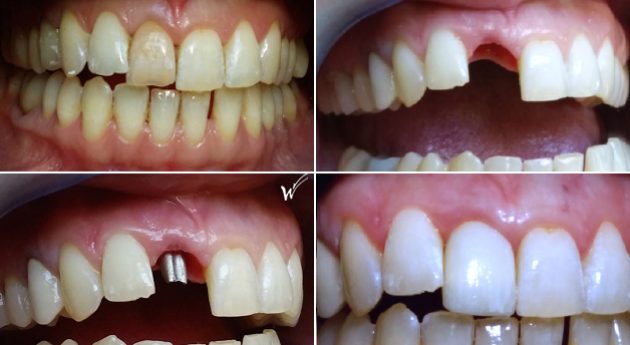
5. L’UTILISATION DE PRF DANS LA POSE D’IMPLANT DENTAIRE
L’utilisation du PRF favorise l’angiogénèse et la cicatrisation tissulaire autour des implants.
L’action des PRF est bénéfique sur la cicatrisation osseuse pendant l’ostéointégration des implants et aussi sur l’amélioration des tissus mous autour de ceux-ci.
Les protocoles de traitement sont accélérés. Le maintien à long terme est optimisé grâce à la qualité accrue des tissus durs et mous.
Les implants dentaires sont progressivement devenus la norme pour le remplacement des dents manquantes. Aujourd’hui, nonobstant les aléas possibles, l’ostéointégration osseuse implantaire n’est plus considérée comme une probabilité mais comme une quasi-certitude.
L’attention des praticiens est désormais focalisée sur la rapidité et la qualité de l’ostéointégration. Les techniques chirurgicales visent à améliorer la qualité osseuse afin d’optimiser la stabilité primaire au moment de la pose de l’implant.
La conséquence est un raccourcissement du délai de mise en charge de l’implant : mise en charge précoce à 6 semaines ou mise en charge immédiate.
Les thérapeutiques chirurgicales ont ainsi été optimisés comme par exemple la stabilité esthétique à long terme, qui dépend notamment du biotype parodontal, c’est à dire la qualité de la gencive, de la quantité et de la qualité de l’os supportant l’implant dentaire.
La gestion des tissus gingivaux entourant l’implant dentaire et de sa restauration, est un enjeu majeur. Il est maintenant reconnu que la vascularisation de l’os et des tissus gingivaux entourant l’implant dentaire est essentielle pour la stabilité à long terme. Les tendances passées et actuelles se sont concentrées sur l’os et son augmentation en tant que clés du succès de l’implant.
Pour cette raison, il est essentiel de veiller à ce que les sites implantés soient gérés de manière appropriée afin d’optimiser l’os et les tissus gingivaux.
L’apport du PRF et du PRP est fondamentale dans cette démarche puisque les concentrés sanguins plaquettaires favorisent de façon significative l’angiogenèse, c’est dire la prolifération des vaisseaux sanguins des tissus dans lesquelles ils sont placés. De ce fait, l’apport du PRP ou du PRF dans les tissus gingivaux et osseux induit une nouvelle vascularisation et augmente la qualité et la vitalité des ces tissus dits “mous” et “durs”.
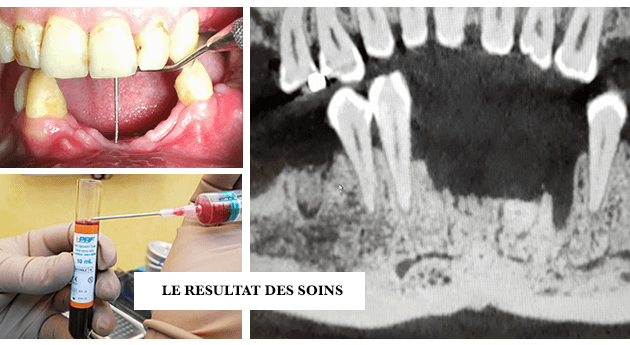
6. L’UTILISATION DE PRF DANS LA RÉGÉNÉRATION OSSEUSE GUIDÉE (ROG)
La Régénération Osseuse Guidée joue un rôle de premier plan dans la dentisterie régénérative depuis le milieu de 1980.
Le principe de la Régénération Osseuse Guidée ROG (i.e. GBR) est sous tendue par l’utilisation de membranes de collagène barrières qui empêchent l’infiltration du tissus osseux par le tissu gingival dont la croissance rapide est en compétition avec le tissu osseux minéralisé à croissance plus lente.
Ces concepts sont largement utilisés dans la reconstruction osseuse en chirurgie orale pré implantaire.
Les protéines morphogénétiques osseuses (Bone morpho protein ou BMP) sont considérées comme la référence pour faciliter une nouvelle formation osseuse. En particulier la BMP 2. Pour autant, une vague de recherche utilisant les concentrés plaquettaires autologue (PRP et PRF) a démontré l’optimisation de l’angiogenèse post chirurgicale avec
L’utilisation du PRP liquide, en raison de l’incorporation d’anticoagulants est discutable dans le cas de ROG puisque la présence du caillot de fibrine est prépondérante.
La deuxième génération de concentré de plaquettes autologues (PRF) a été utilisé en dentisterie, en raison de ses protocoles de préparation sous forme de membrane de fibrine. Le PRF a été développée en tant que membranes de nouvelle génération pour les procédures de ROG.
L’ostéo-conduction et la biocompatibilité des greffons osseux ainsi que des membranes barrières résorbables (ou non) ont été largement débattus dans la littérature. Désormais, les biomatériaux en tant que greffons osseux ne sont plus utilisés en tant que matériaux passifs : mélangé aux PRF, ils ont acquis l’avantage supplémentaire d’être activé par les propres cellules sanguines cicatricielles et les facteurs de croissance du patient. En exploitant les éléments sanguins inducteurs de la formation d’os, les biomatériaux sont devenus bioactifs.
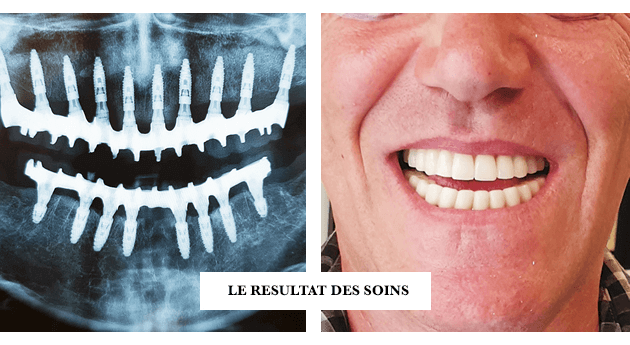
7. LA MISE EN CHARGE IMMÉDIATE D’UNE PROTHÈSE COMPLÈTE GRÂCE AU PRF
La réhabilitation dentaire des patients présentant un édentement complet reste un défi majeur pour le praticien.
On estime maintenant que plus de 20% de la population âgée de 65 ans et plus, subit une perte complète des dents. Avec le vieillissement croissant de la population, ce nombre ne fera que continuer à augmenter.
Dans le protocole du Dr Alain Simonpieri, la stabilité primaire des implants dentaires dans de l’os natif est optimisée par la pose d’une prothèse immédiate (arcade dentaire complète transvissée). Elle réduit les micro-mouvements à moins de 200 microns. C’est le socle de la technique.
Les techniques chirurgicales implantaires de mise en charge immédiatement après la pose d’implants dentaires permettent d’augmenter leur taux de survie ainsi que l’esthétique gingivale grâce à une immobilisation très précoce des implants.
Le but a atteindre est de maintenir une stabilité à long terme des implants et de l’esthétique de la prothèse. L’utilisation de fibrine autologue riche en plaquettes (PRF) sous sa forme de membrane (A-PRF) et injectable (I-PRF) en tant qu’agents biologiques capables d’induire une vascularisation précoce des tissus osseux et des tissus mous, optimise ce but. C’est à dire que l’apport de a-PRF et de i-PRF dans cette technique chirurgicale permet d’optimiser l’objectif principal qui est de parvenir à optimiser l’ostéointégration et la stabilité à long terme des tissus durs et mous autour des implants afin de préserver l’esthétique.


8 . L’UTILISATION DE PRF DANS L’ESTHÉTIQUE ET LE RAJEUNISSEMENT DU VISAGE
Le développement des protocoles de centrifugation à des vitesses plus basses que pour le PRP, a permis la mise au point d’un Plasma Rich Fibrin liquide qui peut être injectable dans les tissus mous, le I-PRF.
Il peut être utilisé en tant que substitut autologue aux thérapies classiques par le PRP. Contrairement à ce dernier, il présente l’avantage de ne contenir aucun additif, ni anti-coagulants-inhibiteurs connus de la régénération des tissus.
L’injections de I-PRF dans le derme ou le tissus conjonctif du visage est indéniablement un protocole majeur dans les thérapies de rajeunissement de la peau.
Par ailleurs, ces injections autour ou dans les cicatrices est particulièrement efficace pour la réduction des cicatrices chéloïdes ou des cicatrices d’acné.
On note le nombre croissant de dentistes qui se forment en esthétique du visage. Plus la population continue de vieillir, plus elle est également préoccupée par son apparence esthétique. Une utilisation croissante de produits comprenant du Botox, des acides hyaluroniques, des fils de PDO et du plasma riche en plaquettes (PRP), entre autres, a été utilisée pour les procédures de rajeunissement du visage.
On estime à présent que plus de 16 millions de procédures esthétiques sont pratiquées chaque année aux États-Unis et cette tendance devrait continuer à augmenter avec le vieillissement de la population. Les techniques sont plus pratiques, plus économiques et plus sûres.
9. UTILISATION DE PLASMA RICH FIBRIN DANS LES DOMAINES DE LA MÉDECINE
Le Plasma Rich Fibrin (PRF) est largement utilisé en chirurgie dentaire, mais elle est appliquée beaucoup plus souvent en médecine générale pour diverses indications.
– Le PRF a tout d’abord été utilisés pour le traitement des ulcères douloureux au niveau des jambes. Il a également été démontré qu’ils amélioraient une variété d’ulcères des jambes et des mains ;
– Le PRF est utilisés en chirurgie plastique et médecine esthétique pour soigner les défauts des tissus mous du visage, rhytides superficielles (rides), cicatrices d’acné, procédures chirurgicales à la lipostructure ;
– Le PRF est utilisé en ORL pour cicatriser les perforations traumatiques aiguës du tambour auriculaire ;
– Le PRF est utilisé en orthopédie et rhumatologie pour soigner les blessures au tendon, l’arthrose du genou, les déchirures chroniques de la coiffe des rotateurs en rhumatologie ;
– Le PRF est utilisé en chirurgie générale pour la gestion de la cholécystectomie laparoscopique, la réparation du prolapsus vaginal, la réparation de fistule urétra-cutanée ;
Ces indications ne sont qu’un aperçu des nombreuses indications du PRF pour la régénération étendue à travers divers domaines de la médecine en dehors du domaine dentaire.
Tous les jours, de nouvelles applications sont découvertes. L’histoire de la médecine et de la dentisterie régénérative ne fait que commencer.

VOUS ÊTES UNIQUE !
APPLICATIONS CLINIQUES DE LA DENTISTERIE RÉGÉNÉRATIVE RÉGÉNÉRATION TISSULAIRE ET PRF
QUELS SONT LES COMPOSANTS BIOLOGIQUES DU PRF (PLATELET RICH FIBRIN)
Les composants biologiques du PRF (Platelet Rich Fibrin): Les facteurs de croissance et leur action sur l’activité cellulaire.
Au cours du processus naturel de cicatrisation, le sang joue un rôle central dans la régénération tissulaire en fournissant divers types de cellules sanguines, facteurs de croissance, cytokines et facteurs de coagulation.
Le concept des PRP, comme celui des PRF, est l’accélération et la potentialisation par les agents sanguins naturels autologues des processus de cicatrisation ou de régénération naturels du corps.
Tout cela grâce à des techniques d’injections de doses supra physiologiques de plaquettes contenant les facteurs moléculaires inducteurs de la régénération tissulaire.
Le PRP (Plasma riche en plaquettes) a été initialement développées pour augmenter le nombre de plaquettes dans les sites cicatriciels. Mais l’utilisation d’anticoagulants d’origine animal ne rend pas optimal ce protocole, même si la guérison est jugée, elle, quasi optimale.
Le concentré de deuxième génération appelé PRF (Fibrin Rich en Platelet) a donc été mis au point comme vue précédemment.
LES AVANTAGES DU PRF
Premier avantage: il est 100% naturel avec aucun anticoagulant exogène
Au fil des ans, de nombreuses découvertes ont permis de comprendre que la fibrine agit sur l’ancrage de différents types de cellules et permet ainsi une libération lente et progressive des facteurs de croissance par ces cellules.
Il a été démontré que cette libération améliorait l’angiogénèse, le comportement des cellules cicatrisantes et donc la régénération des tissus.
Deuxième avantage, il optimise l’ingénierie tissulaire
Il fournit les trois clés fondamentales pour optimiser l’ingénierie tissulaire, à savoir :
Comme le PRP, le PRF contient beaucoup de plaquettes sanguines. La préparation du PRF avec une modification de la vitesse de centrifugation et du temps de centrifugation permet un enrichissement en éléments du groupe cellulaire plasmatique cicatrisant. Il a été démontré que l’abaissement de la vitesse et du temps de centrifugation augmentaient le nombre de macrophages et de leucocytes. Ces cellules sont importantes pour la défense de l’hôte et la cicatrisation des plaies.
Ces cellules sanguines jouent un rôle majeur dans la cicatrisation des plaies car elles sécrètent beaucoup de facteurs de croissance capables d’induire la migration, la prolifération et la différenciation cellulaire. Ces plaquettes et ces cellules du groupe cicatricielle comme les leucocytes sécrètent un grand nombre de facteurs moléculaires inducteurs de la régénération et de la croissance tissulaire.
Notamment :
- Le facteur de croissance transformant-B1 ou Transforming Growth Factor (TGF-B1) ;
- Le facteur de croissance dérivé des plaquettes ou Platelet-Derived Growth factor (PDGF) ;
- Le facteur de croissance endothélial vasculaire ou Vascular Endothelial Growth Factor (VEGF) ;
- Le facteur de croissance-type insuline ou Insulin-like Growth Factor-1 (IGF-1), capable de promouvoir d’avantage la migration, la prolifération et la différenciation des cellules.
Le PRF contient 100% des leucocytes du prélèvement contre 10 à 50% des leucocytes pour le PRP selon le matériel utilisé.
Les anticoagulants n’étant pas utilisés pour la préparation de PRF, un échafaudage tridimensionnel de fibrine est formé, de manière entièrement biologique et naturelle. Au fil des ans, de nombreuses découvertes ont permis de comprendre que la et
La recherche scientifique a permis de comprendre que ce caillot de fibrine à deux actions simultanées :
- Retenir prisonnier les différents types de cellules sanguines nécessaires à la cicatrisation : la fibrine agit sur l’ancrage de différents types de cellules.
- Les facteurs de croissance sont relargués graduellement dans le temps tant en quantité que dans leur nature : l’ancrage cellulaire dans la matrice de fibrine permet une libération lente et progressive des facteurs de croissance par ces cellules.
Ce relargage des facteurs de croissance, avec une quantité et une nature différente dans le temps, à été démontré comme induisant les comportements cellulaires, permettant l’angiogenèse et in fine la régénération tissulaire.
Ainsi, on peut facilement voir que les PRF permettent au corps à guérir plus vite et plus efficacement.
QUELS SONT LES PROTOCOLES DE FABRICATION DU PRF ET LEURS ÉVOLUTIONS?
L’ÉVOLUTION DES TECHNIQUES DE FABRICATION DU PRF VERS LE CONCEPT DE CENTRIFUGATION À BASSE VITESSE
Au cours des cinq dernières années, de nouvelles modifications de la vitesse et du temps de centrifugation ont amélioré les protocoles de fabrication du PRF. Un nouveau concept s’est imposé désormais appelé «concept de centrifugation à basse vitesse».
La diminution de la vitesse de centrifugation du sang fraîchement prélevé sur le patient dans des tubes spécialement adaptés a permis de collecter un nouvel ensemble de cellules, à savoir principalement les leucocytes.
Le concept de centrifugation à basse vitesse (LSCC) introduit l’idée qu’avec la réduction de la force de centrifugation appliquée ou RCF (Relevant Centrifugation Forces) la matrice de fibrine emprisonne un nombre accru de cellules inflammatoires cicatrisantes et de plaquettes, elles même, contenant les facteurs de croissance.
L’Advanced PRF (A-PRP) et l’Advanced PRF plus (A-PRF +) prennent la forme de matrices solides, qui est la base du PRF.
L’A-PRF + préparé selon le concept du LSCC, comparé au PRF, présente un nombre accru de plaquettes et de leucocytes. Il montre des concentrations de libération de facteur de croissance significativement plus élevées sur 10 jours.
De plus, une réduction supplémentaire du RCF basée sur le concept du LSCC a permis la mise au point d’un PRF injectable (i-PRF) sans utiliser d’anticoagulants. Des tubes de prélèvement sanguin spéciaux retardant naturellement, sans apport d’anticoagulants, l’organisation de la matrice de fibrine permet une utilisation clinique, dans un délai court, mais raisonnable.
L’i-PRF, préparé avec le RCF le plus faible, comprend le plus grand nombre de leucocytes et de plaquettes, illustrant l’effet du LSCC sur ce système de concentré de sang.
Les leucocytes sont les principaux protagonistes de la cicatrisation et du processus de régénération. Leur présence dans les matrices d’Advanced PRF et Injectable-PRF met en évidence l’amélioration de leur capacité de régénération. Les nouveaux protocoles de fabrication de matrices de A-PRF et les injections de I-PRF ont un large éventail d’applications cliniques en dentisterie, en chirurgie maxillo-faciale ainsi que dans d’autres domaines médicaux.
En raison de leur protocole de préparation simplifié, minimalement invasif, l’efficacité de ce système s’impose comme une évidence.
LE PROTOCOLE D’OBTENTION DES PRF (J.CHOUKROUN, SCHLEICHER 2000)
Comment prépare t-on les PRF?
Le sang est composé de 99% de globules rouges, de 0,2% de globules blancs et de 0,6-1% de plaquettes (thrombocytes) servant à la coagulation du sang.
Un prélèvement sanguin sur le patient d’un jusqu’a 4 flacons de 10 ml (quantité minime par rapport au volume total de sang et équivalente à une prise de sang classique) est effectué.
La centrifugation des flacons de sang permet de séparer ses composants et de récupérer un concentré riche en plaquettes.
Une partie sert à la préparation d’une fine membrane d’environ 1mm d’épaisseur qui servent à recouvrir les sites chirurgicaux.
Une autre partie peut être mélangée à l’os autogène, allogène, xénogène ou alloplastique (synthétique) qui est utilisé pour combler le défaut osseux.
Utilisations cliniques : Les comblement de sinus avec selon les cas la possibilité de pose immédiate d’implant, les comblements de déficit osseux après une extraction, la cicatrisation des tissus mous après la mise en place d’implant.
Conclusion : Grâce au travail de l’ingénierie génétique de ces 10 dernières années, la régénération de l’os se fait plus vite, en plus grande quantité et qualité et avec une marge sécurité par rapport aux autres méthodes.
Les techniques chirurgicales utilisée sont optimisées par l’apport de concentré plaquettaire autologue.
Le PRP ou Plasma Rich Platelet est un système diffusé par la société REGENLAB validée le Professeur Meningaud (Hopital Henry Mondor)
Le PRF ou Platelet Rich Fibrin est un protocole de récupération développé par le docteur J.Choukroun.
Quelques autres techniques de centrifugation du sang : Plasma Rich in Growth Factors ou P.R.G.F (Anitua 1999)




